先导编辑可以精确安装基因组替换,插入和删除在生命系统中。然而,高效地在体外和体内递送先导编辑组件仍然是一个挑战。
2024年1月8日,博德研究所刘如谦(David R. Liu)团队在Nature Biotechnology 在线发表题为“Engineered virus-like particles for transient delivery of prime editor ribonucleoprotein complexes in vivo”的研究论文,该研究报道了先导编辑器工程病毒样颗粒(PE-eVLPs),它可以传递先导编辑蛋白、先导编辑向导RNA和作为瞬态核糖核蛋白复合物的单向导RNA。
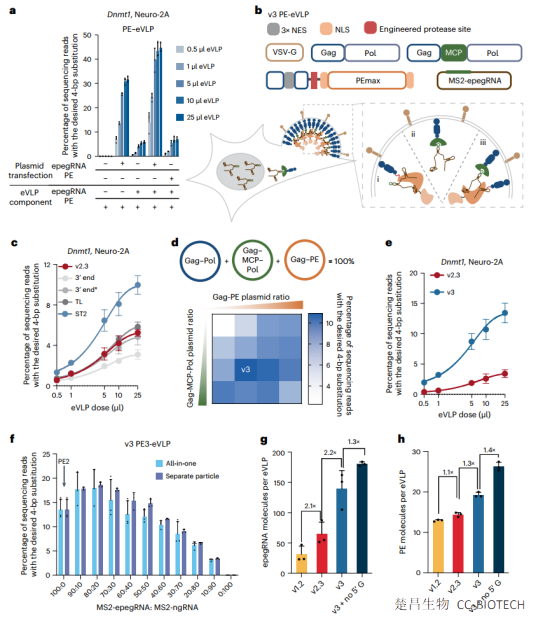
与基于先前报道的碱基编辑器eVLP架构的PE-eVLP结构相比,该系统地设计了v3和v3b PE-eVLPs,其在人类细胞中的编辑效率提高了65至170倍。在两种遗传性失明小鼠模型中,单次注射v3b PE-eVLPs导致视网膜中与治疗相关的先导编辑水平,蛋白质表达恢复和部分视觉功能恢复。优化后的PE-eVLPs支持先导编辑核糖核蛋白在体内的瞬时递送,通过减少脱靶编辑和消除致癌转基因整合的可能性,提高了先导编辑的潜在安全性。